Kryoskopické stanovenie mólových hmotností
04. August, 2010, Autor článku: Valent Ivan, Prírodné vedy
Ročník 3, číslo 8  Pridať príspevok
Pridať príspevok
 Kryoskopia bola v minulosti významnou metódou merania molárnych hmotností a laboratóriách sa používala pomerne často aj dnes. Kryoskopicky sa molárna hmotnosť stanovuje len pre dobre rozpustné neprchavé látky, ktoré vroztoku nepodliehajú disociácii alebo asociácii a nevytvárajú molekulové zlúčeniny s rozpúšťadlom. Teplotu tuhnutia prakticky neovplyvňuje prípadná zmena atmosférického tlaku počas merania. Ďalšou výhodou je, že sa pracuje pri nízkych teplotách, pri ktorých je značne malá prchavosť rozpúšťadiel a nehrozí nebezpečenstvo zmeny koncentrácie vyparovaním počas experimentu.
Kryoskopia bola v minulosti významnou metódou merania molárnych hmotností a laboratóriách sa používala pomerne často aj dnes. Kryoskopicky sa molárna hmotnosť stanovuje len pre dobre rozpustné neprchavé látky, ktoré vroztoku nepodliehajú disociácii alebo asociácii a nevytvárajú molekulové zlúčeniny s rozpúšťadlom. Teplotu tuhnutia prakticky neovplyvňuje prípadná zmena atmosférického tlaku počas merania. Ďalšou výhodou je, že sa pracuje pri nízkych teplotách, pri ktorých je značne malá prchavosť rozpúšťadiel a nehrozí nebezpečenstvo zmeny koncentrácie vyparovaním počas experimentu.
Úvod
Kryoskopia je metóda na stanovenia mólovej hmotnosti látok, založená na znížení bodu tuhnutia roztoku voči čistému rozpúšťadlu (kryoskopické zníženie). Zníženie bodu tuhnutia závisí od koncentrácie rozpustenej látky (vzťah 1), presnejšie od počtu častíc v roztoku, ide o tzv. koligatívnu vlastnosť roztokov:
| (1) |
kde Kkr je kryoskopická konštanta [K mol-1 kg], je molalita rozpustenej látky [mol kg-1], t.j. látkové množstvo látky rozpustené v 1 kg rozpúšťadla. Kryoskopická konštanta je charakteristickou veličinou pre dané rozpúšťadlo. Dá sa určiť experimentálne alebo vypočítať z tepla topenia čistého rozpúšťadla, jeho teploty topenia/tuhnutia (T) a mólovej hmotnosti
| (2) |
kde Mroz je mólová hmotnosť rozpúšťadla a ΔHtop skupenské teplo topenia. Kryoskopická konštanta nadobúda hodnoty napr. 1,855 K mol-1 kg pre vodu a 5,12 K mol-1 kg pre benzén. Ak máme k dispozícii sériu meraní ΔTK pre rôzne koncentrované roztoky so zvyšujúcim sa návažkom rozpustenej látky (m), možno jej mólovú hmotnosť (M) určiť so závislosti ΔTK od m, ktorá je podľa vzťahu (1) lineárna:
| (3) |
kde mroz je hmotnosť rozpúšťadla a a smernica tejto závislosti. Smernicu a určíme lineárnou regresiou experimentálnej závislosti ΔTK od m a hľadanú hodnotu mólovej hmotnosti potom jednoducho vypočítame vzhľadom na vzťah (3):
| (4) |
Pri stanovení mólovej hmotnosti kryoskopickou metódou je dôležité presné meranie teploty a účinné chladenie. V minulosti sa používal na meranie rozdielu teplôt do 5 K s presnosťou 0,005 K dômyselne skonštruovaný Beckmannov teplomer. Tento teplomer má dva zásobníky s ortuťou, takže po adjustácii sa môže používať pri nižších teplotách (kryoskopia), ale aj na meranie rozdielov teplôt varu (ebulioskopia). Súčasná elektronika nám ponúka niekoľko možností ako nahradiť zraniteľný a trochu nepohodlný Beckmannov teplomer. Na presné meranie teploty možno použiť termistory, platinové odporové teplomery (Pt100, Pt1000), alebo teplotné prevodníky na báze integrovaných obvodov (napr. AD590).
Podobne aj pôvodné chladenie meraných roztokov v termoske s ľadom sa dá efektívne nahradiť chladiacim modulom s využitím Peltiérovho článku. Táto súčiastka (obr. 1) je tvorená kaskádou striedavo prepojených polovodičových teliesok typu P a N a je schopná pri prechode prúdu vytvárať teplotný rozdiel medzi jej okrajovými plochami (tzv. Peltiérov efekt) pričom sa jedna strana ochladzuje a druhá zohrieva. Pre dosiahnutie optimálnej účinnosti chladenia je nutné odpadové teplo z teplej strany Peltiérovho článku odvádzať napr. pomocou chladiča na procesory osobných počítačov.
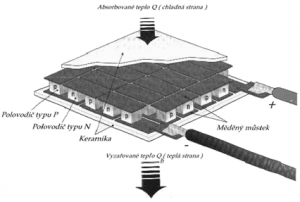
Obr. 1. Schéma Peltiérovho článku.
V tejto práci je kryoskopia aplikovaná na stanovenie mólovej hmotnosti gáfru v rozpúšťadle benzéne. Gáfor je terpenoid so sumárnym vzorcom C10H16O a štruktúrou znázornenou na obr. 2. Určenie mólovej hmotnosti známej látky nám umožní porovnať získanú hodnotu M s presnou hodnotou a urobiť tak závery o presnosti použitej metódy.
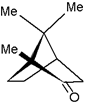
Obr. 2. Štruktúrny vzorec gáfru.
S javmi spojenými s kryoskopiou sa môžme stretnúť aj v bežnom živote. Predchádzanie námrazy ciest pomocou soľného posypu ja azda najznámejším príkladom kryoskopického efektu, keď soľný roztok zamŕza pri nižšej teplote ako „čistá“ voda. Ďalším príkladom praktického využitia kryoskopie sú prístroje na meranie osmotického tlaku, osmometre, ktoré pracujú na princípe merania teploty tuhnutia meranej vzorky.
Úlohy:
- Zmerajte teplotu tuhnutia benzénu a piatich roztokov s rôznou hmotnosťou pridaného gáfru.
- Zostrojte graf závislosti kryoskopického zníženia roztokov od hmotnosti gáfru.
- Určte smernicu nameranej závislosti a vypočítajte mólovú hmotnosť gáfru. Porovnajte ju so skutočnou hodnotou a stanovte relatívnu chybu merania.
Aparatúra:
COBRA3 Basic Unit + Temperature Modul (PHYWE), odporový teplomer Pt100, mosadzný blok, elektromagnetické miešadlo MR 1000 (Heidolph), Peltiérov článok TEC1 12708 (72 W), zdroj jednosmerného prúdu NP-9615 (HADEX), chladič na procesory, digitálne váhy AM50 (Axis), BlueTooth (MSI) 2 ks, osobný počítač.
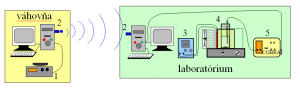
Obr. 3. Schéma kryoskopickej aparatúry. 1 – váhy, 2 – BlueTooth, 3 – zdroj na napájanie Peltiérovho článku, 4 – zariadenie na meranie teploty tuhnutia, 5 – meracie zariadenie COBRA3 Basic Unit.
Schéma aparatúry je na obr. 3. Peltiérov článok je s mosadzným blokom a chladičom spojený prostredníctvom vodivej pasty. Ostatné steny bloku sú od okolia izolované polystyrénom. Merania teploty prebiehajú na prístroji COBRA3, ktorý je spojený s laboratórnym osobným počítačom cez sériový port a ovládaný pomocou programu Measure. Druhý osobný počítač je vo váhovni spojený s digitálnymi váhami taktiež sériovým portom a pomocou prenosových kľúčov BlueTooth (USB port) zabezpečuje bezdrôtovú komunikáciu medzi váhami a osobným počítačom v laboratóriu.
Softvér:
Windows98 (Microsoft), Excel 2003 (Microsoft), Kryos 3.2 (aplikácia Excel, I. Valent), Measure 4.0.1.0 (PHYWE).
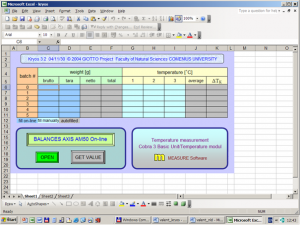
Obr. 4. Aplikácia Kryos na ovládanie kryoskopických meraní.
Meranie a spracovávanie dát je organizované excelovskou aplikáciou Kryos (obr. 4), v rámci ktorej je možné získavať a automaticky spracovávať údaje z váhovne a spúšťať program Measure na meranie teploty. Hodnoty teplôt sa automaticky spriemernia a vypočíta sa kryoskopické zníženie. Aplikácia využíva tzv. makrá v programovacom jazyku VBA (Visual Basic for Aplications).
Pomôcky:
skúmavka s plochým dnom (priemer 35 mm), magnetické miešadielko, pinzeta, odmerný valec, lodička, nádobka na váženie kvapalín, exsikátor.
Chemikálie:
benzén, gáfor
UPOZORNENIE!!!Benzén je zaradený do zoznamu karcinogénov a práca s ním vyžaduje maximálnu opatrnosť. Vhodnejším rozpúšťadlom je cyklohexán.
Postup:
Do skúmavky s plochým dnom diferenčne odvážime ~30 ml benzénu. S benzénom pracujeme len v digestóriu! Skúmavku s miešadielkom vložíme do chladiaceho bloku a uzavrieme zátkou s odporovým teplomerom. Pre zvýšenie tepelnej vodivosti medzeru medzi vonkajším plášťom skúmavky a mosadzným blokom opatrne vyplníme destilovanou vodou. Spustíme miešanie a napájanie Peltiérovho článku nastavíme na prúd ~3 A pri napätí ~6 V. Spustíme aplikáciu Kryos a program Measure. Ak teplota v skúmavke poklesne na ~7 oC, začneme registráciu teploty od času.
Teplota spravidla klesá až pod bod tuhnutia, potom náhle stúpne v dôsledku uvoľnenia kryštalizačného tepla. Tento efekt sa dá pozorovať aj voľným okom, keď sa číra kvapalina náhle zakalí. Po ~40 s od kryštalizácie záznam teploty zastavíme a vyhodnotíme teplotu tuhnutia ako priesečník priamok stúpajúcej a klesajúcej (ustálenej) fázy teplotnej závislosti od času. Po roztopení vzorky (ak treba, skúmavku zahrejeme spustením napájania Peltiérovho článku s opačnou polaritou), meranie opakujeme. Každú hodnotu teploty tuhnutia získame ako priemer troch meraní.
Potom do benzénu pridáme diferenčne odvážený (presne) gáfor (~0,3 g) a proces merania teploty tuhnutia znovu trikrát opakujeme. Pridáme ďalších presne odvážených ~0,3 g gáfru atď. Takto získame priemerné teploty tuhnutia piatich roztokov gáfru v benzéne. Medzi jednotlivými váženiemi gáfru lodičku odložíme do exsikátora vo váhovni. Po skončení meraní, pinzetou vyberieme miešadielko, roztok zo skúmavky vylejeme v digestóriu do nádoby s organickým odpadom a skúmavku aj s miešadielkom dôkladne vypláchneme prúdom vody v umývadle.
Vyhodnotenie:
Teplota tuhnutia roztokov sa na rozdiel od čistého rozpúšťadla počas ochladzovania mení (klesá). Príčinou je vymŕzanie rozpúšťadla a tým zakoncentrovávanie roztoku. Preto je potrebné správnu teplotu tuhnutia roztoku určiť ako priesečník priamok, ako je to znázornené na obr. 5.
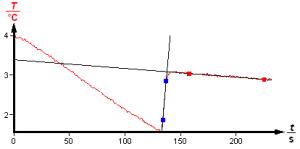
Obr. 5. Vyhodnotenie teploty tuhnutia roztoku.
Lineárnou regresiou (metódou najmenších štvorcov; najlepšie priamo v Exceli) určíme smernicu závislosi ΔTK od m (obr. 6). Hľadanú hodnotu mólovej hmotnosti M vypočítame z hodnoty smernice podľa vzťahu (4).
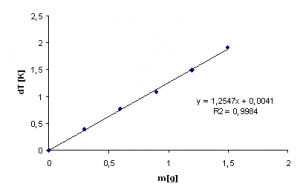
Obr. 6. Lineárna regresia závislosti kryoskopického zníženia od hmotnosti rozpustenej látky.
Literatúra:
- V. Kellö, A. Tkáč: Fyzikálna chémia, Alfa 1977, s. 348.
- http://www.leybold-didactic.de/ga/6/667/6674971/6674971e.pdf
- M. Dřínek:
http://www.hw.cz/Teorie-a-praxe/Dokumentace/ART652-Peltierovy-termobaterie.html
Spoluautormi článku sú M. Matejdes, J. Benko, Katedra fyzikálnej a teoretickej chémie PriF UK

